Оглавление
EMDN – принципы, структура, доступ
EMDN (Европейская номенклатура медицинских изделий) является официальной номенклатурой, установленной Европейской комиссией для использования производителями медицинских изделий в целях регистрации в ЮДАМЕД база данных. Самая первая его версия была выпущена на 4й Май 2021 г. В целом, номенклатура предназначена для поддержки всех видов деятельности, предусмотренных МЛУ и IVDR, а также для предоставления пациентам/покупателям важной информации об устройствах. По мнению экспертов, переход на номенклатуру EMDN является наиболее эффективным и удачным выбором для европейских структур здравоохранения на данный момент.
На чем основан EMDN?
Согласно официальной информации, опубликованной Европейской комиссией, в основе EMDN лежат 8 ключевых принципов:
Под руководством регулятора – управление, валидация, а также процессы обновления и консультирования по номенклатуре поддерживаются и контролируются регулирующими органами
Структурированный – прозрачные иерархии, которые могут быть сгруппированы в группы и типы
Предсказуемый – стабильная структура с возможностью различного использования и развития технологий
Прозрачный - потребности здравоохранения и пациентов отражены в обновлениях
включительно – широкая открытость периодических обзоров
Доступный – термины, описания и коды полностью доступны для всех
Доступный – номенклатура может быть использована любым производителем без платы/комиссии
Международный – идентифицированы на международном уровне с даты применения MDR/IVDR
Как устроена EMDN?
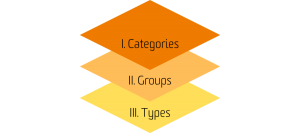
EMDN имеет семиуровневую буквенно-цифровую структуру. Медицинские изделия позиционируются на три основных уровня:
Буквенно-цифровой код для конкретного медицинского изделия представляет собой комбинацию букв и цифр каждого уровня, максимально 13 цифр.
Как получить к нему доступ?
Как было указано в принципах, EMDN доступен для всех заинтересованных сторон*. Вы могли получить к нему доступ здесь >>
*Производители, пациенты, исследовательские организации, практикующие врачи, больницы, аптеки и т. д.
Если ваша компания должна иметь дело с регистрацией в EUDAMED или любым другим бизнесом, связанным с регулированием MDR - назначьте бесплатную встречу с нашими экспертами >>
Источники:
https://ec.europa.eu/health/md_eudamed/latest_updates_en
https://link.springer.com/article/10.1007/s12553-021-00567-1