Оглавление
Ознакомьтесь с требованиями SFDA и спецификацией Track & Trace для Саудовской Аравии
Саудовская Аравия является одним из наиболее динамично развивающихся фармацевтических рынков в регионе MENA. По оценкам, к 2026 году рынок достигнет 11 миллиардов долларов США, что почти равно размеру Египта и ОАЭ вместе взятых. COVID-19 повлиял на рынок наркотиков в Саудовской Аравии, стимулируя его рост, и ожидается, что среднегодовой темп роста в течение прогнозируемого периода (2020-2027 гг.) составит 7,3%. Внедрение системы отслеживания и отслеживания в Саудовской Аравии является частью программы правительства Саудовской Аравии Vision 2030.
Проект трансформации здравоохранения реализуется с 2018 года и ставит перед собой три цели: улучшить доступ, качество и ценность. Более того, в отличие от Европы, полная система отслеживания включает внедрение процессов агрегации. К 2030 году Саудовская Аравия хочет отслеживать все лекарства и товары медицинского назначения, зарегистрированные для использования человеком внутри страны и за рубежом. К 2030 году Минздравом останется орган регулирования здравоохранения, поскольку «это будет одно из крупнейших преобразований в сфере здравоохранения в мире с точки зрения количества центров, численности обслуживаемого населения и сложности».
Управление по контролю за продуктами и лекарствами Саудовской Аравии (SFDA) опубликовало версию 6.1 Спецификации штрих-кодирования лекарств, в которой содержится информация о последних требованиях и рекомендациях по сериализации и агрегации. SFDA считает, что стандартизированная система идентификации от производства до доставки пациентам необходима для удовлетворения растущей потребности в целостности и отслеживаемости продукции, одобряя внедрение стандартов GS1.
Основные отмеченные возражения направлены на следующее:
Повышение безопасности пациентов
Уменьшить количество ошибок при приеме лекарств
Включите отслеживание каждой единицы лекарственного средства в цепочке поставок, что приведет к:
- Обнаружение подделок
- Обеспечить отслеживаемость и быстрый отзыв и изъятие продукции
- Обеспечить точный поток информации в режиме реального времени между заинтересованными сторонами
- Поддержка оптимального использования лекарств
Требования к сериализации
Все маркировки лекарственных средств должны быть заменены линейными штрих-кодами на штрих-коды GS1 Data Matrix, включая следующие:
- GTIN
- Дата истечения срока действия
- Серийный номер
- Серийный номер
Требования к агрегации
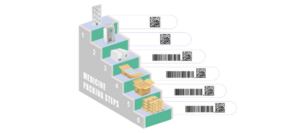
Производитель должен выполнять агрегирование на разных уровнях упаковки, чтобы дистрибьютору, вплоть до цепочки поставок, было проще отслеживать и сообщать в SFDA о каждой единице движения лекарства без необходимости сканирования отдельной коробки с лекарством.
- Вторичная упаковка — GTIN, срок годности, номер партии, уникальный серийный номер на каждой коробке
- Картонная/коробочная упаковка – линейный штрих-код или матрица данных GS1, закодированная с помощью SSCC или GTIN + SN; GTIN + SN будет использоваться только с однородным случаем/мультфильмом
- Поддон — линейный штрих-код или матрица данных GS1, закодированная с помощью SSCC или GTIN +SN; GTIN +SN будет использоваться только с однородным поддоном.
* Однородный: коробка или поддон будут содержать только препараты одного типа.
** Гетерогенные: в коробке или поддоне будут находиться препараты другого типа.
Список продуктов
Продукты, которые требуют использования штрих-кодов для сериализации и агрегации:
- Лекарства для человека, упакованные и готовые к продаже
- Расфасованные и готовые к продаже травяные продукты и товары для здоровья в будущем потребуют штрихового кодирования.
- Ветеринарные фармацевтические продукты, которые упакованы и готовы к продаже, в будущем потребуют штрихового кодирования.
Исключения составляют бесплатные образцы фармацевтической продукции, незарегистрированные лекарства, заказанные больницами для конкретных пациентов и в определенных количествах, лекарства, разрешенные для личного использования, и лекарства, изъятые для переупаковки.
Источники:
https://www.sfda.gov.sa/sites/default/files/2021-03/DrugBarcodingSpecificationsEN.pdf