Tibbiy asboblar
Traceability tibbiy asboblar va in vitro qurilmalarning umumiy sifatini monitoring qilish, nazorat qilish va yaxshilashda muhim rol o'ynaydi.
Evropa Ittifoqi qoidalari
2017 yilda Tibbiy asboblarni tartibga solish (MDR) nashr etildi va MDDdan AIMDDga o'tishning to'rt yillik sayohatining boshlanishini belgiladi. 2021-yil 26-maydan boshlab MDR toʻliq amal qiladi. MDR tibbiy asboblarni ishlab chiqarish, tarqatish yoki sotib olish sohalariga ta'sir qiladi.
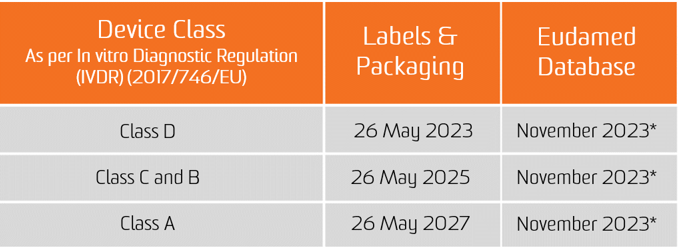
The In vitro diagnostika reglamenti (IVDR) 2017-yil 25-mayda kuchga kirdi. 2022-yil 26-maydan boshlab yangi qurilmalar Yevropa bozoriga joylashtirilishi uchun IVDR talablariga javob berishi kerak. Tasdiqlangan organ tomonidan allaqachon sertifikatlangan mahsulotlar bozorga 2024-yil 25-maygacha baʼzi shartlar ostida va ishlab chiqaruvchi IVDRda belgilangan muayyan talablarni bajarsa, sotilishi mumkin.
UDI nima?
UDI (Noyob Qurilma identifikatsiyasi)
The UDI global miqyosda qabul qilingan qurilmani identifikatsiyalash va kodlash standarti orqali yaratilgan raqamli yoki alfanumerik belgilar qatoridir. Bu bozorda ma'lum bir qurilmani aniq identifikatsiya qilish imkonini beradi. UDI UDI-DI va UDI-PIdan iborat.
 UDI-DI (GS1 ekvivalenti GTIN – Global savdo elementi raqami)
UDI-DI (GS1 ekvivalenti GTIN – Global savdo elementi raqami)
UDI-DI qurilma modeliga xos noyob raqamli yoki alfanumerik kod bo'lib, UDI ma'lumotlar bazasida saqlanadigan ma'lumotlarga "kirish kaliti" sifatida ham qo'llaniladi.
 UDI- PI (GS1 Ekvivalent AI – Ilova identifikatorlari)
UDI- PI (GS1 Ekvivalent AI – Ilova identifikatorlari)
UDI-PI - bu qurilma ishlab chiqarish birligini aniqlaydigan raqamli yoki alfanumerik kod.
UDI-PI ning har xil turlari qator raqami, lot raqami, dasturiy ta'minot identifikatsiyasi, ishlab chiqarish yoki yaroqlilik muddati yoki ikkala turdagi ma'lumotlarni o'z ichiga oladi.
UDI amalga oshirish
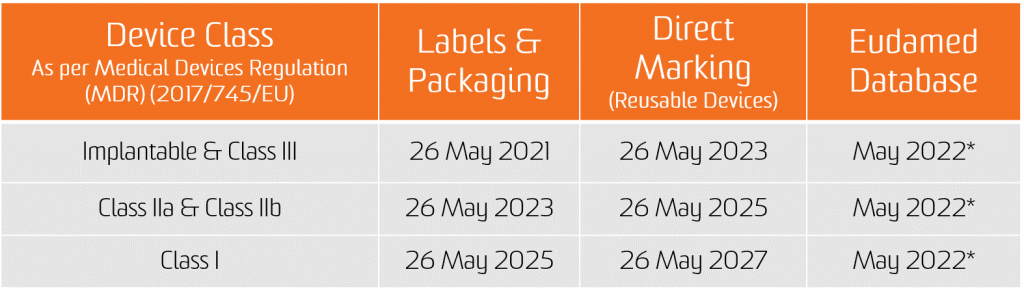
UDI topshirig‘i bo‘yicha majburiyat ikkita yangi Qoidalar qo‘llanilgan kundan boshlab, ya’ni tibbiy asboblar uchun 2021-yil 26-may va In Vitro diagnostik tibbiy asboblar uchun 26-maydan boshlab amal qiladi.
EUDAMED maʼlumotlar bazasiga UDI maʼlumotlarini taqdim etish majburiyati tibbiy asboblar uchun 2022-yil 26-noyabrdan va in vitro diagnostik tibbiy asboblar uchun 2023-yil 26-noyabrdan boshlab amal qiladi (agar EUDAMED tegishli Nizom qoʻllanilishi sanasidan oldin toʻliq ishlagan boʻlsa; aks holda bu majburiyat EUDAMED to'liq ishlay boshlaganidan keyin 24 oy o'tgach amal qiladi).
Shu bilan birga, ishlab chiqaruvchilar tibbiy asboblar uchun 2021-yil 26-maydan va 2022-yil 26-maydan boshlab In Vitro diagnostik tibbiy asboblar uchun roʻyxatdan oʻtish majburiyatlarini ixtiyoriy ravishda bajarishlari mumkin.
Shuni ta'kidlash kerakki, Eudamed to'liq ishlayotgan bo'lsa, tibbiy asboblar uchun 2021 yil 26 maydan va In Vitro diagnostik tibbiy asboblar uchun 2022 yil 26 maydan keyin istalgan vaqtda asboblar to'liq ro'yxatga olinadi (MDR 29-moddasi va IVDR 26-moddasi). Eudamedda ularning tegishli jiddiy hodisasini ro'yxatdan o'tkazish uchun dastlabki shart bo'lib qolmoqda.
* 2020 yil 11-noyabrdagi CAMD nashrida aytilishicha, Evropa Komissiyasi huquqiy sabablarga ko'ra Eudamed-ning ishga tushirilishi 2022 yil mayigacha kechiktirilishini e'lon qiladi. Eudamed uchun yangi ishga tushirish sanasi 2022-yil 26-mayda kuchga kiradigan In Vitro diagnostika reglamentini amalga oshirish sanasiga to'g'ri keladi.
EUDAMED nima?
Tibbiy asboblar bo'yicha yangi tartibga soluvchi Evropa ma'lumotlar bazasi
Eudamed - MDR va IVDR qoidalariga muvofiq milliy vakolatli organlar va Komissiya o'rtasida ma'lumot almashish uchun markaziy ombor vazifasini bajaradigan xavfsiz veb-ga asoslangan portal.
Eudamedning asosiy roli quyidagi majburiyatlarni o'z ichiga oladi:
Eudamed ro'yxatdan o'tish
UDI/Qurilmalarni ro'yxatdan o'tkazish
Xabardor organlardan sertifikatlarni oling va ko'ring
Klinik tekshiruvlar va samaradorlik tadqiqotlari ma'lumotlarini taqdim eting
Hushyorlik va bozordan keyingi kuzatuv haqida xabar bering
Bozor nazorati faoliyati
Tibbiy asboblar qoidalariga oid barcha veb-seminarlarni tomosha qiling
[Veb-translyatsiya]: GS1 va SoftGroup tomonidan tibbiy asboblar uchun UDI talabini qondirish