Evropa Ittifoqi FMD haqida umumiy ma'lumot
2011 yil iyul oyida e'lon qilingan Soxta dori vositalari bo'yicha direktiva (FMD) bilan Evropa dori agentligi (EMA) Evropa Ittifoqi mamlakatlarida kuzatuv standartlari boshlanishini o'rnatdi.
The Soxtalashtirilgan dorilar bo'yicha direktiv (2011/62/EU direktivasi) dori-darmonlarni qalbakilashtirishga qarshi kurashish va dori vositalarining xavfsizligini ta'minlash va savdo aylanmasida dori vositalarining qat'iy nazorat qilinishini ta'minlash uchun muvofiqlashtirilgan Evropa choralarini joriy qiladi. Chora-tadbirlar quyidagilarni o'z ichiga oladi:
- Dori vositalarining tashqi qadoqlarida majburiy xavfsizlik belgilari - noyob identifikator va buzilishlarga qarshi vosita
- Yuridik onlayn dorixonalarni aniqlash uchun umumiy, Evropa Ittifoqi bo'ylab logotip
- Faol farmatsevtik ingredientlarni import qilish bo'yicha qat'iy qoidalar
- Ulgurji distribyutorlar uchun hujjatlarni yuritish talablari kuchaytirildi
2019 yildan boshlab barcha farmatsevtika mahsulotlari FMD majburiyatlarini to'liq bajarishi kerak. 2025 yilgacha Gretsiya va Italiya kabi alohida tizimga ega bo'lgan Evropa Ittifoqi mamlakatlari farmatsevtika treklari va izlari qoidalariga to'liq mos kelishi kerak.
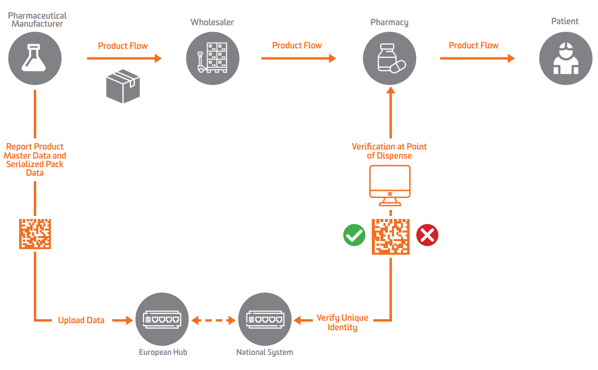
Seriyalashtirish talablari
Evropa Ittifoqi FMD ma'lumotlariga ko'ra, ketma-ketlik Evropada ikkilamchi yoki sotiladigan birlik darajasida paydo bo'lishi kerak. Tasdiqlashni yoqish uchun ishlab chiqaruvchilar avval mahsulotni seriyalashtirishi va ketma-ketlashtirilgan ma'lumotlarni unga qarshi so'rovlarni amalga oshirishi mumkin bo'lgan markaziy omborga yuborishi kerak.
Seriyalashtirish, tekshirish va vakolatli organlarga hisobot berishni yoqish uchun EI FMD ishlab chiqaruvchilardan paketlarni to'rtta ma'lumot elementi bilan belgilashni talab qiladi, ular inson o'qishi mumkin bo'lgan shaklda chop etilishi va GS1 2D DataMatrixda kodlangan va saqlanishi kerak:
- Mahsulot identifikatori
- Ishlab chiqarish raqami
- Partiya yoki partiya raqami
- Quyidagi sanagacha foydalanilsin
Maʼlumotlarning beshinchi elementidan — milliy toʻlov raqamidan foydalanish ixtiyoriydir va Yevropa Ittifoqidagi bir nechta davlatlar ijtimoiylashtirilgan tibbiyot dasturi doirasida dori vositasining toʻlovini bogʻlash uchun uni noyob identifikatorga kiritishni soʻrashi mumkin.
Farmatsevtika ishlab chiqaruvchilari va parallel savdogarlar kerak maʼlumotlarni Yevropa Ittifoqining markaziy markaziga xabar qilish tomonidan boshqariladi Evropa dori vositalarini tekshirish tashkiloti (EMVO), shuningdek, foydalanuvchilarni Hubga kiritadi. Bu ma'lumotlarni oxirgi foydalanuvchini ishga tushirish va milliy tizimlarning ishlashi uchun mas'ul bo'lgan tegishli milliy dori vositalarini tekshirish tashkilotlari (NMVO) tomonidan boshqariladigan tegishli ma'lumotlar omborlariga tushiradi.
Hisobotga qo'yiladigan talablar
Evropa Ittifoqi FMD bo'yicha, Marketing Ruxsat egasi (MAH) mahsulot asosiy ma'lumotlarini va seriyali mahsulot to'plami ma'lumotlarini taqdim etishi kerak.
Asosiy ma'lumotlar quyidagilarni o'z ichiga oladi:
- Mahsulot kodlari
- Shakl
- Kuch
- Paket uchun dozalar
- Paket turi
- Tarqatish uchun maqsadli bozor(lar).
- Kelajak va mahsulot asosiy ma'lumotlariga har qanday yangilanishlar
Seriyalashtirilgan mahsulot to'plami ma'lumotlariga quyidagilar kiradi:
- Mahsulot kodlari
- Partiya/partiya raqami
- Quyidagi sanagacha foydalanilsin
- Seriya raqamlari
- Seriyalashtirilgan mahsulot to'plami ma'lumotlariga har qanday yangilanishlar
