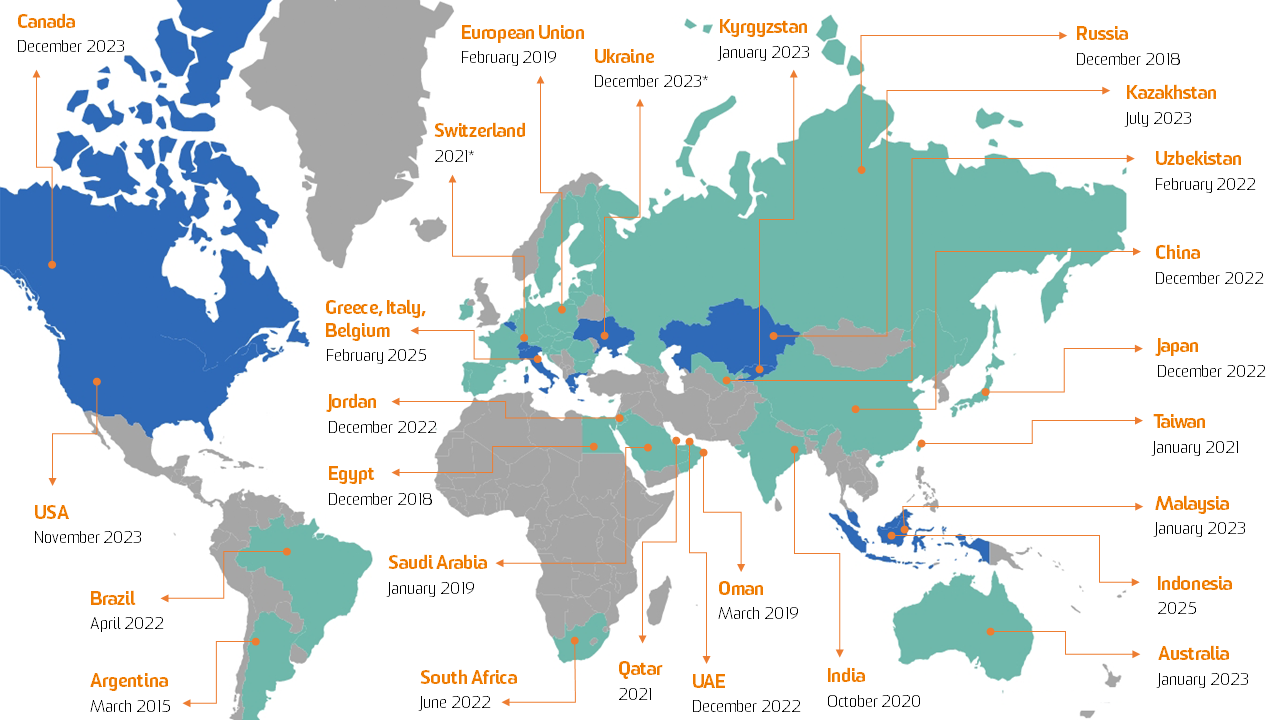
Globale Serialisierungslandschaft
Die Serialisierung ist bereits in so unterschiedlichen Ländern wie Argentinien, Australien, Bahrain, Brasilien, China, Ägypten, Indien, Jordanien, Oman, Katar, Russland, Saudi-Arabien, Südkorea, Taiwan, den Vereinigten Arabischen Emiraten, Usbekistan und der EU* erforderlich.

Die Herausforderungen von Track & Trace
Die unterschätzte Investition für die Implementierung der Serialisierung in die Produktionsprozesse hat viele Pharmaunternehmen vor unerwartete Herausforderungen gestellt, wie zum Beispiel:
Mangel an einheitlicher Kommunikation im Unternehmensnetzwerk
Zusätzliche Investitionen in die IT-Infrastruktur
Einschränkung der Produktionseffizienz und Mangel an qualifiziertem Personal
Manuelle Arbeit an Serialisierungsdatendateien
Unzureichender Support-Service
Die perfekte Lösung für Ihre Serialisierungsanforderungen
 Einfache Integration mit mehreren Anbietern auf Ebene 3
Einfache Integration mit mehreren Anbietern auf Ebene 3
 Automatischer Serialisierungsdatenaustausch
Automatischer Serialisierungsdatenaustausch
 Unbeeinflusste Produktionseffizienz
Unbeeinflusste Produktionseffizienz
 Einfaches Onboarding von Partnern (CMOs, MAHs, Wholesales)
Einfaches Onboarding von Partnern (CMOs, MAHs, Wholesales)
 Automatische Kommunikation mit externen Kundenschnittstellen wie ERP, WMS
Automatische Kommunikation mit externen Kundenschnittstellen wie ERP, WMS
 Benutzerfreundliches Bedienfeld
Benutzerfreundliches Bedienfeld
 Funktion zur automatischen Veröffentlichung von Daten
Funktion zur automatischen Veröffentlichung von Daten
 Automatische Konvertierung von Serialisierungsdateien
Automatische Konvertierung von Serialisierungsdateien
 Ein Ansprechpartner für alle Serialisierungsfragen
Ein Ansprechpartner für alle Serialisierungsfragen
 Alle Teilnehmer der pharmazeutischen Kette können die Originalität und Herkunft der von ihnen vertriebenen Produkte überprüfen
Alle Teilnehmer der pharmazeutischen Kette können die Originalität und Herkunft der von ihnen vertriebenen Produkte überprüfen
Sie vertrauen uns aus einem bestimmten Grund



 SoftGroup stellte eine sehr klare, einfache und benutzerfreundliche Technologieplattform bereit und schuf eine Umgebung, die auf Zusammenarbeit und gegenseitiger Verantwortung basierte. Als relativ kleines Unternehmen ist es wichtig, einen Partner zu haben, der in der Lage ist, Ihr Unternehmen und die spezifischen Bedürfnisse der Menschen zu verstehen, die mit den bereitgestellten Tools arbeiten müssen. Unserer Erfahrung nach hat SoftGroup diese Umgebung geschaffen und erweist sich eindeutig als zuverlässiger und sachkundiger Partner für unsere Serialisierungsanforderungen.
SoftGroup stellte eine sehr klare, einfache und benutzerfreundliche Technologieplattform bereit und schuf eine Umgebung, die auf Zusammenarbeit und gegenseitiger Verantwortung basierte. Als relativ kleines Unternehmen ist es wichtig, einen Partner zu haben, der in der Lage ist, Ihr Unternehmen und die spezifischen Bedürfnisse der Menschen zu verstehen, die mit den bereitgestellten Tools arbeiten müssen. Unserer Erfahrung nach hat SoftGroup diese Umgebung geschaffen und erweist sich eindeutig als zuverlässiger und sachkundiger Partner für unsere Serialisierungsanforderungen.
Paul van Spring
Verkaufs und Marketing Direktor
Wir sind auf einen Klick entfernt.
Wir sind entschlossen, das Wachstum Ihres Unternehmens zu unterstützen.
Vereinbaren Sie einen Discovery-Anruf, der uns hilft, Ihren speziellen Fall besser zu verstehen.
Klicken Sie hier, um ein Meeting zu planen





