Panorama global de serialización
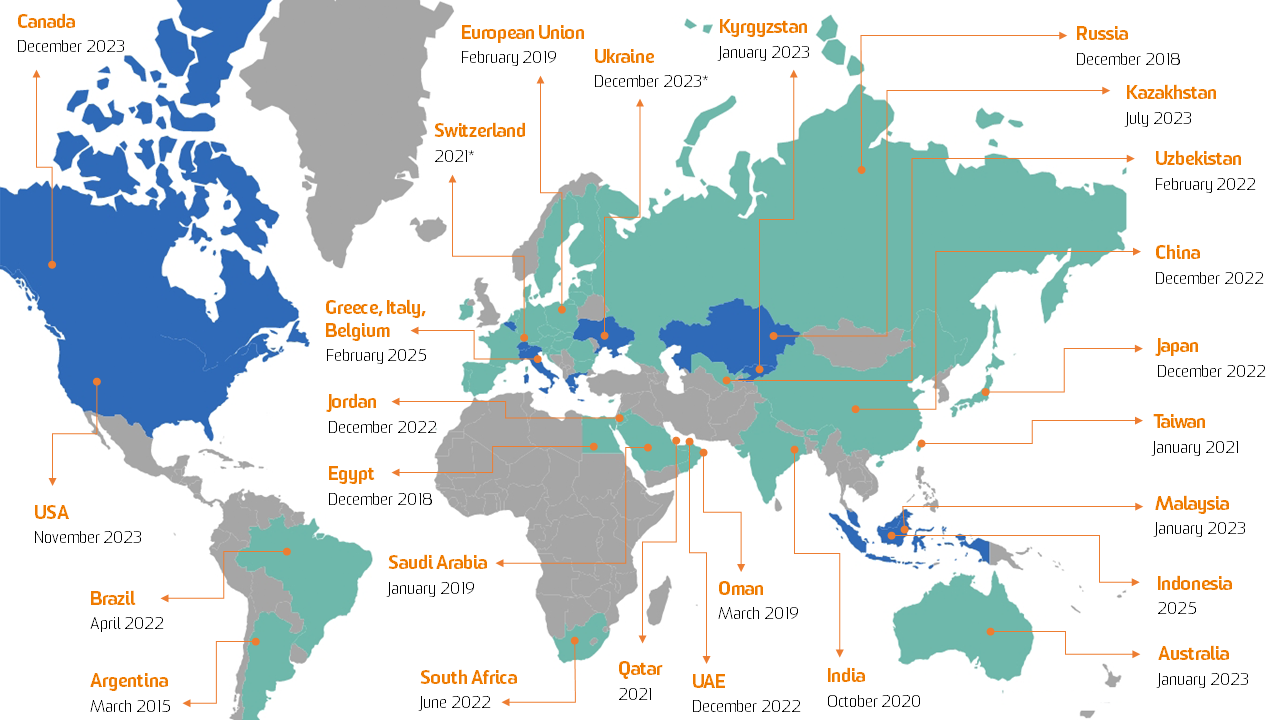
La serialización ya se requiere en países tan diversos como Argentina, Australia, Baréin, Brasil, China, Egipto, India, Jordania, Omán, Qatar, Rusia, Arabia Saudita, Corea del Sur, Taiwán, Emiratos Árabes Unidos, Uzbekistán y la Unión Europea*.

Los desafíos de Track & Trace
La inversión subestimada para la implementación de la serialización en los procesos de producción ha llevado a muchas compañías farmacéuticas a desafíos inesperados como:
Falta de comunicación unificada entre la red empresarial.
Inversión adicional en infraestructura de TI
Limitación de la eficiencia productiva y falta de personal calificado
Trabajo manual en archivos de datos de serialización
Servicio de soporte insuficiente
La opción perfecta para sus necesidades de serialización
 Fácil integración con múltiples proveedores en el nivel 3
Fácil integración con múltiples proveedores en el nivel 3
 Intercambio automático de datos de serialización
Intercambio automático de datos de serialización
 Eficiencia de producción no afectada
Eficiencia de producción no afectada
 Fácil incorporación de socios (CMO, TAC, mayoristas)
Fácil incorporación de socios (CMO, TAC, mayoristas)
 Comunicación automática con la interfaz del cliente externo como ERP, WMS
Comunicación automática con la interfaz del cliente externo como ERP, WMS
 Interfaz amigable
Interfaz amigable
 Función de publicación automática de datos
Función de publicación automática de datos
 Conversión automática de archivos de datos de serialización
Conversión automática de archivos de datos de serialización
 Un punto de contacto para todos los problemas de serialización
Un punto de contacto para todos los problemas de serialización
 Todos los participantes de la cadena farmacéutica pueden verificar la originalidad y procedencia de los productos que comercializan
Todos los participantes de la cadena farmacéutica pueden verificar la originalidad y procedencia de los productos que comercializan
Ellos confían en nosotros por una razón



 SoftGroup proporcionó una plataforma tecnológica muy clara, simple y fácil de usar y creó un entorno basado en la colaboración y la propiedad mutua. Como empresa relativamente pequeña, es importante contar con un socio que tenga la capacidad de comprender su empresa y las necesidades específicas de las personas que necesitan trabajar con las herramientas proporcionadas. Según nuestra experiencia, SoftGroup ha creado este entorno y claramente demuestra ser un socio confiable y bien informado para nuestras necesidades de serialización.
SoftGroup proporcionó una plataforma tecnológica muy clara, simple y fácil de usar y creó un entorno basado en la colaboración y la propiedad mutua. Como empresa relativamente pequeña, es importante contar con un socio que tenga la capacidad de comprender su empresa y las necesidades específicas de las personas que necesitan trabajar con las herramientas proporcionadas. Según nuestra experiencia, SoftGroup ha creado este entorno y claramente demuestra ser un socio confiable y bien informado para nuestras necesidades de serialización.
Paul van Sprang
Director de Ventas y Marketing
Estamos a un clic de distancia.
Estamos decididos a apoyar el crecimiento de su negocio.
Programe una llamada de descubrimiento que nos ayudará a comprender mejor su caso específico.
Haga clic aquí para programar una reunión





