Общий обзор системы отслеживания и отслеживания в России
Россия начала трансформацию своей фармацевтической цепочки поставок 29 декабря 2017 года, когда Президент подписал Федеральный закон № 425-ФЗ. Этот закон направлен на оптимизацию контроля качества фармацевтических препаратов, защиту от поддельных лекарств и мониторинг предложения, спроса и расходов.
По правилам в Федеральный закон № 425-ФЗ, систему прослеживаемости уточнил и анонсировал «Честный знак» (Обязательная маркировка товаров – официальный сайт торговой маркировки Честный ЗНАК | Регистрация в национальной системе Честный ЗНАК (xn--80ajghhoc2aj1c8b.xn--p1ai)) отраслевым органам, таким как производители, дистрибьюторы и т. д.
Основное требование к системам прослеживаемости заключается в том, чтобы компании подключались и соблюдали требования Национальной цифровой системы отслеживания и прослеживания «Честный знак», которая находится в ведении Центра исследований перспективных технологий (ЦРПТ) и, как ожидается, будет полностью заработает к 2024 году. К 2024 году практически все потребительские товары, продаваемые, производимые или импортируемые, должны быть маркированы.
Правила распространяются на несколько категорий товаров: лекарства, антисептики, медицинские приборы, пищевые добавки, молочные продукты, напитки, бутилированная вода, пиво и напитки на его основе, табак, инвалидные коляски, легкая промышленность, обувь, мех, парфюмерия, шины, фотокамеры и лампы-вспышки. . В стадии эксперимента находится отслеживание осетровой и лососевой икры, изделий из титанового металла, а также велосипедов и велосипедов, подлежащих маркировке средствами идентификации. Требования различаются в зависимости от отрасли, но для всех них есть некоторые общие потоки, такие как коды DataMatrix, криптокоды, сериализация, агрегирование, отчетность и управление записями.
В России действуют одни из самых строгих в мире правил цепочки поставок через Национальную цифровую систему отслеживания и отслеживания, известную как Честный ЗНАК.
По сравнению с европейскими требованиями, российская система сериализации более сложна, так как каждое местонахождение продукта в цепочке поставок в России должно быть сообщено в государственную базу данных.
Правила цифровой маркировки лекарственных средств — Track & Trace for Medicines
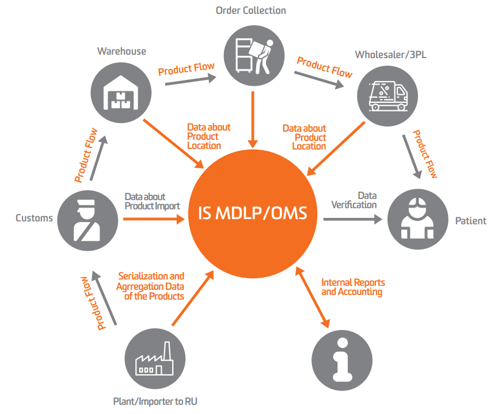
Для реализации системы отслеживания лекарственных средств создана специализированная информационная система контроля обращения фармацевтической продукции (ИС МДЛП). Система предназначена для использования в сфере здравоохранения и эксплуатируется Центром исследований перспективных технологий (ЦРПТ).
Этот процесс цифровой маркировки предназначен для предотвращения производства и обращения контрафактной и фальсифицированной продукции.
Код маркировки Data Matrix наносится на вторичный (розничный) уровень упаковки. При отсутствии вторичной упаковки код наносится на первичную упаковку.
Матрица 2D-данных:
- Код продукта/ GTIN
- Серийный номер
- Ключ проверки (т. е. криптоключ)
- Код подтверждения (т. е. криптокод)
Читаемая человеком часть:
- GTIN
- Серийный номер (SN)
- Лот (номер партии)
- Дата окончания срока
Код маркировки запрашивается у оператора через регистратор выбросов, и система выдает код в течение двух часов.
Цена кода маркировки утверждена Постановлением Правительства РФ от 8 мая 2019 года № 577 и составляет 0,5 рубля без учета НДС.
Немаркированные упаковки, произведенные до даты введения обязательной маркировки, могут реализовываться до окончания срока годности фармацевтической продукции.
Система отслеживания присваивает каждому продукту уникальный код Data Matrix. Каждый код зашифрован, чтобы гарантировать невозможность его массового копирования или подделки.
Сроки
В соответствии с требованиями Федерального закона от ДД. 12 апреля 2010 г. (ред. от 04 июня 2018 г.) с 01 января 2020 г. введена обязательная маркировка лекарственных средств. 14 декабря 2018 года «Об особенностях внедрения системы отслеживания лекарственных средств для медицинского применения» с 01 июля началась обязательная регистрация участников обращения в учетной записи пользователя ИС МДЛП для лекарственных средств из перечня дорогостоящих нозологий. С 01 октября 2019 года маркировка лекарственных средств 7ВЗН стала обязательной.
