在本文中,我们将就在法国实施欧盟伪造药品指令 (EU FMD) 时使用全球与国家标准对药品编纂进行一些澄清。
目录
背景
2019 年,GS1 采用了确保其编码系统的唯一标识和完整性的规则,特别是在第三方分配代码时。
GS1 France 随后更新了与国际制药俱乐部 (CIP) 的合同,以符合这些规则。
2021 年 12 月,ANSM(法国国家药品和保健品安全局)、CIP 和 GS1 France 正式签署“三方协议”,将法国医药产品编纂体系维持三年(可能延长一年)。该协议以及法国卫生部的相关法令和命令旨在确保法国的供应链、可追溯性、报销和患者获得药品的机会,并将 CIP 和 UCD 代码纳入法国法律。
用于识别法国市场上授权的药品的代码是:
- 识别每个包装的国家编号,称为“code identifiant de présentation”(CIP 代码)
- 以及(如果适用)标识通用分配单元(通常是初级包装级别)的编号,称为“代码标识 l'unité commune de dispensation”(UCD 代码)。
这些是当前的 13 个字符的代码,前 4 位数字是 GS1 France 自 2006 年以来分配给 CIP 的前缀 3400。该代码符合 ISO/IEC 15459-3 2014 和 ISO/IEC 15459-4 2014,即: ISO认可的GS1标准。
全球与国家药品编纂系统的技术考虑
法国将实施的药品编纂长期解决方案的提案包括:
1. 继续使用基于 GS1 标准的全球标准作为用于供应链/物流目的的代码(即用于市场授权和报销的国家编号),或者使用当前的国家贸易项目编号(NTIN 开头) 3400)或将国家编号映射到全球贸易项目编号(GTIN),如其他欧盟国家实施的那样。
或者
2. 过渡到使用基于CIP代码的国家标准。自 2023 年 5 月起,CIP 被授权 ISO/IEC 15459 发行机构,并且可以生成以前缀 VIP 开头的唯一标识符。
继续使用基于 GS1 标准的全球标准
第一个选项
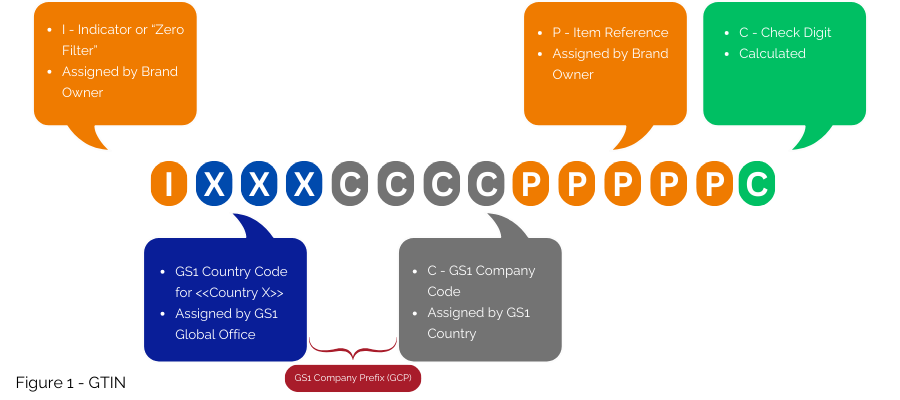
对于像法国这样拥有现有国家编号系统的国家,GS1 提供了过渡到全球统一编号系统的策略。 GS1 建议使用 GTIN(图 1)来实施 EU FMD,主要将其编码在 GS1 DataMatrix 中。如果必须保留国家编号,则可以通过数据库交叉引用检索该编号,而无需将其包含在 GS1 DataMatrix 中。
然而,GS1 认识到,在一些成员国,由于医疗保健系统管理要求或过渡到全球标准的需要,国家编号可能需要以人类可读的格式显示在包装上,而不一定编码在条形码中。
该提案涉及使用转换表将 CIP 代码映射到 GTIN(如比利时所示),并促进其在 GS1 系统中的使用。如有必要,CIP 代码可以以人类可读的格式打印在包装上,而无需像今天在西班牙那样将其编码在条形码中。
第二个选择
第二种选择是将国家编号嵌入到 NTIN 中,而不是使用 GTIN,即使不是最具全球互操作性,但仍可在 GS1 系统中兼容。
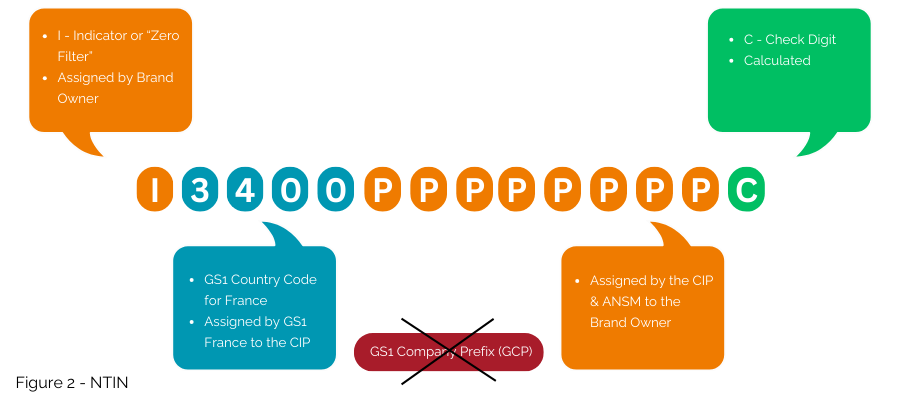
这是目前根据 GS1 France、CIP 和 ANSM 之间的合同实施的解决方案。 GS1 前缀 3400 经 GS1 France 授权给 CIP,允许将 CIP 和 ANSM 颁发的号码作为 NTIN 嵌入到 GTIN 结构中(图 2);然后它就可以在 GS1 系统中使用。
过渡到使用基于 CIP 代码的国家标准
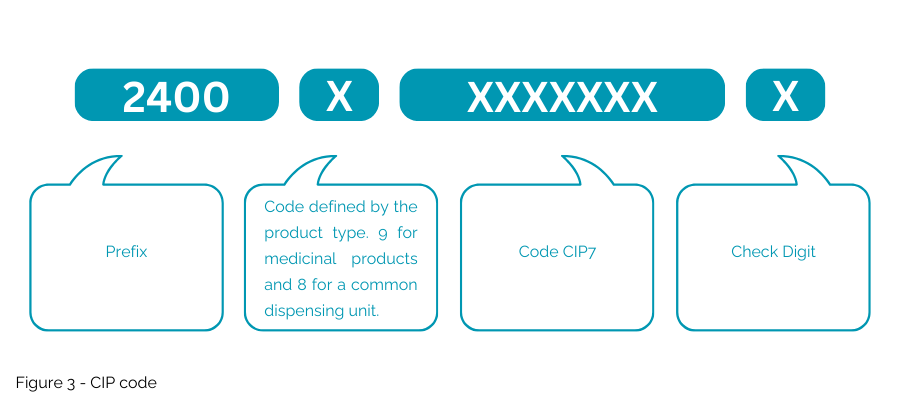
提议的 CIP 代码(图 3)与法国市场当前使用的 NTIN 不同,因为提议的“CIP 代码”不会嵌入到 GS1 密钥中。该国家代码仅在法国接受特定用途,并且不允许使用多市场包装。
CIP代码和NTIN的区别
下面是 GS1 标识符的编码和建议的 CIP 代码的编码之间的比较
1.GS1标识符的编码
- 利用前导 Function One 字符来表示 GS1 DataMatrix 使用,调用 GS1 解码规则。
- 在 NTIN 开头包含 AI (01),以指示后续字符代表 GTIN 或 NTIN(产品代码)。
- 在 Expiration date 的开头加入 AI (17),表示后面的字符代表过期日期。
- 在批号/批号开头使用AI(10),表明后面的字符代表批号/批号。
- 序列号开头使用AI(21),表示后面的字符代表序列号。
2. 拟议CIP代码的编码
- 将被编码到通用 ISO/IEC 数据矩阵中,需要一个新的、特定的数据管理系统。
- 开头使用“1P”作为数据分隔符,表示CIP代码(产品代码); “AI”是 GS1 语法独有的。
- 在到期日期的开头合并“9D”作为数据分隔符。
- 使用“1T”作为批次号开头的数据分隔符。
- 在序列号开头包含“S”作为数据分隔符。
结论 – 实施新的药品编纂的潜在影响
供应给法国的药品标签和包装需要进行修改,以便携带编码 CIP 代码和其他数据属性的通用 ISO 数据矩阵(图 4)。 GS1 DataMatrix 将继续在其他欧盟国家使用(图 5)。
(图片来自关于使用全球与国家标准对药品进行分类以在法国实施欧盟伪造药品指令的讨论文件)
拟议的药品数据编码变更,特别是从 GS1 标准到法国独特的国家编码系统的转变,带来了重大挑战。如果不进行定制升级,现有的扫描、解码和处理系统将无法自动解释新数据矩阵中的数据。这一变化不仅影响制造商,还可能引起整个供应链的动荡,影响已经推迟实施欧盟FMD的医院和药店。
这将破坏法国体系内部以及法国体系与其他欧盟体系之间的互操作性,并对法国药品的获取和当地产业的竞争力构成威胁。
来源: GS1 |关于使用全球与国家标准对药品进行编纂以在法国实施欧盟伪造药品指令的讨论文件