[Blog] Veranderingen in de codificatie van geneesmiddelen in Frankrijk
In dit artikel zullen we enkele verduidelijkingen geven over het gebruik van mondiale versus nationale normen voor de codificatie van geneesmiddelen ter implementatie van de EU-richtlijn voor vervalste geneesmiddelen (EU FMD) in Frankrijk.
Inhoudsopgave
Achtergrond
In 2019 heeft GS1 regels aangenomen om unieke identificatie en integriteit in haar codificatiesysteem te garanderen, vooral wanneer derden codes toekennen.
GS1 France heeft vervolgens zijn contract met de Club Inter Pharmaceutique (CIP) bijgewerkt om aan deze regels te voldoen.
In december 2021 formaliseerden ANSM (Frans Nationaal Agentschap voor de Veiligheid van Geneesmiddelen en Gezondheidsproducten), CIP en GS1 France een “tripartiete overeenkomst” om het Franse geneesmiddelencodificatiesysteem voor drie jaar te handhaven (met een mogelijke verlenging van één jaar). Deze overeenkomst, samen met een daarmee samenhangend decreet en bevel van het Franse Ministerie van Volksgezondheid, heeft tot doel de toeleveringsketen, de traceerbaarheid, de terugbetaling en de toegang van patiënten tot geneesmiddelen in Frankrijk veilig te stellen, waarbij CIP- en UCD-codes in de Franse wetgeving worden opgenomen.
De codes die worden gebruikt om geneesmiddelen te identificeren die op de Franse markt zijn toegelaten, zijn:
- het nationale nummer dat elke verpakking identificeert, genaamd “code identifiant de présentation” (CIP-code)
- en, indien van toepassing, het nummer dat de gemeenschappelijke uitgifte-eenheid identificeert (meestal het niveau van het primaire pakket), genaamd de “code identifiant l'unité commune de dispensation” (UCD-code).
Dit zijn de huidige codes van 13 tekens, waarbij de eerste 4 cijfers het voorvoegsel 3400 zijn dat sinds 2006 door GS1 France aan de CIP is toegewezen. Deze code voldoet aan ISO/IEC 15459-3 2014 en ISO/IEC 15459-4 2014, dwz: GS1-normen erkend door ISO.
Technische overwegingen over een mondiaal versus nationaal systeem voor de codificatie van geneesmiddelen
De voorstellen voor de langetermijnoplossing die in Frankrijk moet worden geïmplementeerd voor de codificatie van geneesmiddelen omvatten:
1. de voortzetting van het gebruik van mondiale standaarden gebaseerd op GS1-standaarden als de code die wordt gebruikt voor supply chain-/logistieke doeleinden (dat wil zeggen met het nationale nummer dat wordt gebruikt voor marktautorisatie en voor terugbetaling), hetzij met het huidige National Trade Item Number (NTIN beginnend met 3400) of door het nationale nummer te koppelen aan een Global Trade Item Number (GTIN) zoals geïmplementeerd in andere EU-landen.
Of
2. de transitie naar het gebruik van een nationale standaard gebaseerd op de CIP-code. Sinds mei 2023 is het CIP erkend ISO/IEC 15459 uitgevende instantie en kan unieke identificatiegegevens genereren, beginnend met het voorvoegsel VIP.
Voortzetting van het gebruik van mondiale standaarden op basis van GS1-standaarden
Eerste optie
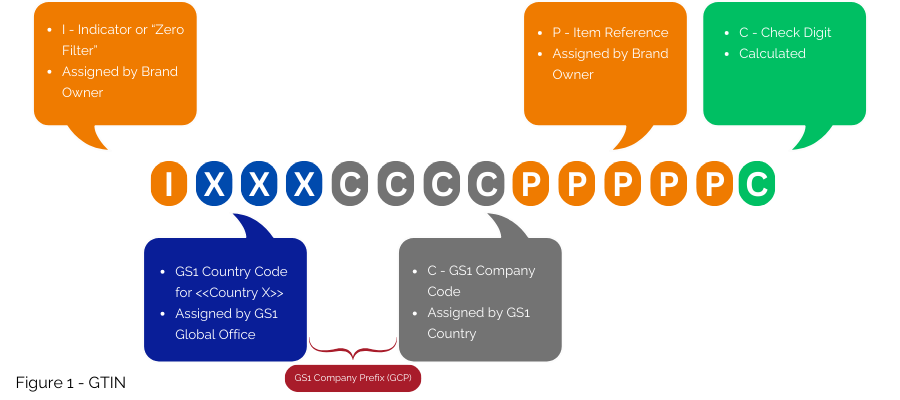
Voor landen als Frankrijk met bestaande nationale nummersystemen biedt GS1 strategieën voor de overgang naar mondiaal geharmoniseerde nummering. GS1 stelt voor om het GTIN (Figuur 1) te gebruiken om de EU-MKZ te implementeren, en deze voornamelijk te coderen in de GS1 DataMatrix. Indien een rijksnummer behouden moet blijven, kan dit via een database-kruisverwijzing worden opgevraagd, zonder dat dit in de GS1 DataMatrix wordt opgenomen.
GS1 erkent echter dat in sommige lidstaten, als gevolg van vereisten op het gebied van het beheer van gezondheidszorgsystemen of de noodzaak om over te stappen op mondiale standaarden, het nationale nummer mogelijk op de verpakking moet worden weergegeven in een voor mensen leesbaar formaat en niet noodzakelijkerwijs gecodeerd in de streepjescode.
Het voorstel omvat het koppelen van de CIP-code aan een GTIN met behulp van een conversietabel, zoals gedemonstreerd in België, en het faciliteren van het gebruik ervan binnen het GS1-systeem. Indien nodig kan de CIP-code in een voor mensen leesbaar formaat op de verpakking worden afgedrukt, zonder deze in de streepjescode te coderen, zoals dat tegenwoordig in Spanje gebeurt.
Tweede optie
De tweede optie, die nog steeds compatibel is binnen het GS1-systeem, ook al is deze niet de meest mondiale interoperabele, is het inbedden van het nationale nummer in een NTIN, in plaats van een GTIN te gebruiken.
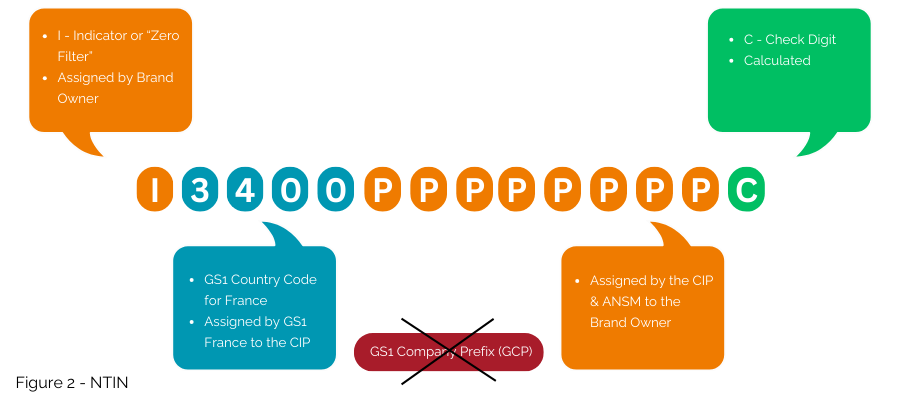
Dit is de oplossing die momenteel wordt geïmplementeerd onder het contract tussen GS1 France, de CIP en de ANSM. Het GS1-voorvoegsel 3400 is door GS1 France in licentie gegeven aan de CIP om het inbedden van het door CIP en ANSM uitgegeven nummer als een NTIN in de GTIN-structuur mogelijk te maken (Figuur 2); het maakt vervolgens het gebruik ervan binnen het GS1-systeem mogelijk.
Overgang naar het gebruik van een nationale standaard op basis van de CIP-code
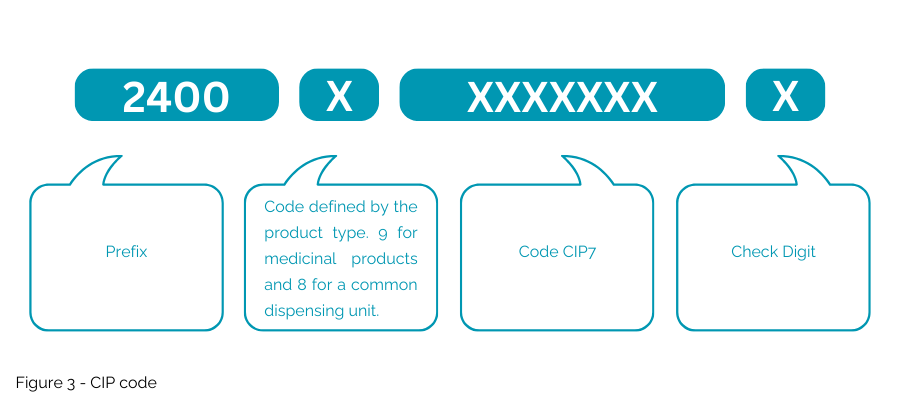
De voorgestelde CIP-code (Figuur 3) verschilt van de huidige NTIN die voor de Franse markt wordt gebruikt, aangezien de voorgestelde “CIP-code” niet in een GS1-sleutel zou worden ingebed. Deze nationale code wordt in Frankrijk alleen geaccepteerd voor specifiek gebruik en staat het gebruik van multimarket-verpakkingen niet toe.
Verschillen tussen CIP-code en NTIN
Hier is een vergelijking tussen de codering van GS1-identificatoren en de codering van de voorgestelde CIP-code
1.Codering van GS1-identificatoren
- Maakt gebruik van een leidend Function One-teken om het gebruik van GS1 DataMatrix aan te duiden, waarbij GS1-decoderingsregels worden aangeroepen.
- Voeg AI (01) toe aan het begin van het NTIN om aan te geven dat de volgende tekens een GTIN of NTIN (productcode) vertegenwoordigen.
- Voeg AI (17) toe aan het begin van de vervaldatum, waarmee wordt aangegeven dat de volgende tekens een vervaldatum vertegenwoordigen.
- Gebruik AI (10) aan het begin van het batch-/lotnummer, om aan te geven dat de volgende tekens een batch-/lotnummer vertegenwoordigen.
- Gebruik AI (21) aan het begin van het serienummer, wat aangeeft dat de volgende tekens een serienummer vertegenwoordigen.
2. Codering van de voorgestelde CIP-code
- Zal worden gecodeerd in een generieke ISO/IEC-datamatrix, waardoor een nieuw, specifiek databeheersysteem nodig is.
- Gebruik “1P” als gegevensscheidingsteken aan het begin om een CIP-code (productcode) aan te geven; “AI” is exclusief voor de GS1-syntaxis.
- Voeg “9D” toe als gegevensscheidingsteken aan het begin van de vervaldatum.
- Gebruik “1T” als gegevensscheidingsteken aan het begin van het batch-/lotnummer.
- Voeg “S” toe als gegevensscheidingsteken aan het begin van het serienummer.
Conclusie – Potentiële impact van de implementatie van een nieuwe codificatie van geneesmiddelen
De etiketten en verpakkingen van aan Frankrijk geleverde geneesmiddelen zullen moeten worden herzien om de generieke ISO-gegevensmatrix (Figuur 4) te kunnen bevatten die de CIP-code en andere gegevensattributen codeert. De GS1 DataMatrix zal in andere EU-landen gebruikt blijven worden (Figuur 5).
(Afbeelding uit discussiestuk over het gebruik van mondiale versus nationale normen voor de condificatie van geneesmiddelen ter implementatie van de EU-richtlijn vervalste geneesmiddelen in Frankrijk)
De voorgestelde veranderingen in de codering van geneesmiddelengegevens, met name de verschuiving van GS1-standaarden naar een uniek nationaal coderingssysteem in Frankrijk, brengen aanzienlijke uitdagingen met zich mee. Bestaande scan-, decoderings- en verwerkingssystemen zullen niet in staat zijn om gegevens binnen de nieuwe Data Matrix automatisch te interpreteren zonder aangepaste upgrades. Deze verandering heeft niet alleen gevolgen voor fabrikanten, maar kan ook turbulentie in de hele toeleveringsketen veroorzaken, met gevolgen voor ziekenhuizen en apotheken die al vertraging hebben opgelopen bij de implementatie van de EU-MKZ.
Dit zou de interoperabiliteit binnen het Franse systeem en tussen het Franse systeem en de andere EU-systemen ondermijnen, maar ook een bedreiging vormen voor de toegang tot geneesmiddelen in Frankrijk en het concurrentievermogen van de lokale industrie.
Bron: GS1 | Discussienota over het gebruik van mondiale versus nationale normen voor de codificatie van geneesmiddelen ter implementatie van de EU-richtlijn vervalste geneesmiddelen in Frankrijk