[Blog] EMDN – was steckt hinter der neuen offiziellen Nomenklatur in der EU?
Inhaltsverzeichnis
EMDN – Prinzipien, Struktur, Zugang
EMDN (Europäische Nomenklatur für Medizinprodukte) ist die offizielle Nomenklatur, die von der Europäischen Kommission zur Verwendung bei der Registrierung von Medizinprodukten durch Hersteller in der EU festgelegt wurde EUDAMED Datenbank. Die allererste Version davon wurde am 4th Mai 2021. Im Allgemeinen soll die Nomenklatur alle darunter liegenden Aktivitäten unterstützen MDR Und IVDR, sowie um den Patienten/Kunden wichtige Informationen zu den Geräten zur Verfügung zu stellen. Basierend auf Expertenmeinungen ist die Übernahme der EMDN-Nomenklatur derzeit die effektivste und erfolgreichste Wahl für europäische Gesundheitsstrukturen.
Worauf basiert EMDN?
Laut den offiziellen Informationen der Europäischen Kommission hat EMDN 8 Schlüsselprinzipien hinter sich:
Reglergeführt – Das Management, die Validierung sowie die Prozesse der Aktualisierung und Beratung zur Nomenklatur werden von den Aufsichtsbehörden unterstützt und kontrolliert
Strukturiert – transparente Hierarchien, die in Gruppen und Typen geclustert werden können
Vorhersagbar – stabile Struktur mit Möglichkeiten für verschiedene Nutzungen und technologische Entwicklung
Transparent – die Bedürfnisse der Gesundheitsfürsorge und der Patienten, die sich in den Aktualisierungen widerspiegeln
Inklusive – große Offenheit regelmäßiger Überprüfungen
Verfügbar – Die Begriffe, Beschreibungen und Codes sind für alle vollständig verfügbar
Zugänglich – Die Nomenklatur kann von jedem Hersteller ohne Gebühr/Provision verwendet werden
International – seit Geltungsbeginn der MDR/IVDR auf internationaler Ebene identifiziert
Wie ist EMDN strukturiert?
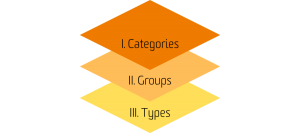
Das EMDN hat eine alphanumerische Struktur mit sieben Ebenen. Medizinprodukte werden in drei Hauptebenen eingeordnet:
Der alphanumerische Code ist für ein medizinisches Gerät eine Kombination aus Buchstaben und Zahlen jeder Ebene, da das Maximum 13 Ziffern beträgt.
Wie greife ich darauf zu?
Wie in den Grundsätzen erwähnt, ist das EMDN für alle Beteiligten verfügbar und zugänglich*. Sie könnten darauf zugreifen hier >>
*Hersteller, Patienten, Forschungseinrichtungen, Praktiker, Krankenhäuser, Apotheken etc.
Wenn Ihr Unternehmen sich mit der Registrierung bei EUDAMED oder anderen Geschäften im Zusammenhang mit der MDR-Verordnung befassen muss – Vereinbaren Sie ein kostenloses Treffen mit unseren Experten >>
Quellen:
https://ec.europa.eu/health/md_eudamed/latest_updates_en
https://link.springer.com/article/10.1007/s12553-021-00567-1