Indice dei contenuti
EMDN – principi, struttura, accesso
EMDN (nomenclatura europea dei dispositivi medici) è la nomenclatura ufficiale, stabilita dalla Commissione Europea per l'utilizzo per la registrazione dei dispositivi medici da parte dei fabbricanti nel EUDAMED Banca dati. La prima versione è stata rilasciata il 4th Maggio 2021. In generale, la nomenclatura ha lo scopo di supportare tutte le attività sotto MDR E IVDR, nonché per fornire ai pazienti/clienti informazioni importanti sui dispositivi. Sulla base dei pareri degli esperti, l'adozione della nomenclatura EMDN è al momento la scelta più efficace e vincente per le strutture sanitarie europee.
Su cosa si basa EMDN?
Secondo le informazioni ufficiali rilasciate dalla Commissione Europea, l'EMDN ha 8 principi chiave dietro di sé:
Regolatore guidato – la gestione, la convalida, nonché i processi di aggiornamento e consulenza sulla nomenclatura sono supportati e controllati dalle autorità di regolamentazione
Strutturato – gerarchie trasparenti che possono essere raggruppate in gruppi e tipologie
Prevedibile – struttura stabile con opportunità per vari usi e sviluppo tecnologico
Trasparente – le esigenze sanitarie e dei pazienti riflesse negli aggiornamenti
Inclusivo – ampia apertura delle revisioni periodiche
Disponibile – i termini, le descrizioni e i codici sono completamente disponibili per tutti
Accessibile – la nomenclatura potrebbe essere utilizzata da qualsiasi produttore senza alcun compenso/commissione
Internazionale – individuati a livello internazionale dalla data di applicazione del MDR/IVDR
Come è strutturato l'EMDN?
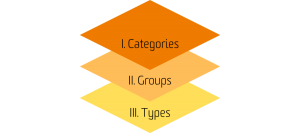
L'EMDN ha una struttura alfanumerica con sette livelli. I dispositivi medici sono posizionati in tre livelli principali:
Il codice alfanumerico per dispositivo medico concreto è una combinazione di lettere e numeri di ogni livello, in quanto il massimo è di 13 cifre.
Come accedervi?
Come indicato nei principi, l'EMDN è disponibile e accessibile a tutte le parti interessate*. Potresti accedervi ecco >>
*Produttori, pazienti, organizzazioni di ricerca, professionisti, ospedali, farmacie, ecc.
Se la tua azienda ha a che fare con la registrazione su EUDAMED o qualsiasi altra attività relativa al regolamento MDR - fissa un incontro gratuito con i nostri esperti >>
Fonti:
https://ec.europa.eu/health/md_eudamed/latest_updates_en
https://link.springer.com/article/10.1007/s12553-021-00567-1