[Blog] EMDN – Que cache la nouvelle nomenclature officielle dans l'UE ?
Table des matières
EMDN – principes, structure, accès
EMDN (Nomenclature Européenne des Dispositifs Médicaux) est la nomenclature officielle, établie par la Commission européenne pour l'enregistrement des dispositifs médicaux par les fabricants dans le EUDAMED base de données. La toute première version est sortie le 4e Mai 2021. De manière générale, la nomenclature est destinée à supporter l'ensemble des activités MDR et IVDR, ainsi que pour fournir aux patients/clients des informations importantes sur les appareils. Sur la base d'avis d'experts, l'adoption de la nomenclature EMDN est le choix le plus efficace et le plus réussi pour les structures de santé européennes à l'heure actuelle.
Sur quoi repose EMDN ?
Selon les informations officielles publiées par la Commission européenne, EMDN a 8 principes clés derrière lui :
Dirigé par le régulateur – la gestion, la validation, ainsi que les processus de mise à jour et de conseil sur la nomenclature sont soutenus et contrôlés par les régulateurs
Structuré – des hiérarchies transparentes qui pourraient être regroupées en groupes et types
Prévisible – structure stable avec possibilité d'utilisations diverses et de développement technologique
Transparent – les soins de santé et les besoins des patients reflétés dans les mises à jour
Compris – large ouverture des revues périodiques
Disponible – les termes, descriptions et codes sont entièrement disponibles pour tout le monde
Accessible – la nomenclature pourrait être utilisée par n'importe quel fabricant sans frais/commission
International – identifié au niveau international depuis la date d'application du MDR/IVDR
Comment est structuré EMDN ?
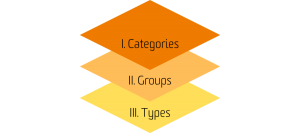
L'EMDN a une structure alphanumérique à sept niveaux. Les dispositifs médicaux sont positionnés en trois niveaux principaux :
Le code alphanumérique pour un dispositif médical concret est une combinaison de lettres et de chiffres de chaque niveau, le maximum étant de 13 chiffres.
Comment y accéder ?
Comme cela a été mentionné dans les principes, l'EMDN est disponible et accessible pour toutes les parties prenantes*. Vous pourriez y accéder ici >>
*Fabricants, patients, organismes de recherche, praticiens, hôpitaux, pharmacies, etc.
Si votre entreprise doit faire face à l'enregistrement sur EUDAMED ou toute autre entreprise liée à la réglementation MDR - planifier une rencontre gratuite avec nos experts >>
Sources:
https://ec.europa.eu/health/md_eudamed/latest_updates_en
https://link.springer.com/article/10.1007/s12553-021-00567-1