
目录
了解沙特阿拉伯的 SFDA 要求和 Track & Trace 规范
沙特阿拉伯是中东和北非地区发展最活跃的医药市场之一。据估计,该市场到 2026 年将达到 110 亿美元,几乎相当于埃及和阿联酋的总和。 COVID-19 影响了沙特药品市场,推动了其增长,预计在预测期内(2020-2027 年)的复合年增长率为 7.3%。在沙特阿拉伯引入跟踪系统是沙特政府 2030 年愿景计划的一部分。
医疗保健转型项目自 2018 年以来一直在进行,设定了三个目标来改善可及性、质量和价值。此外,与欧洲不同,完整的跟踪系统包括引入聚合过程。到 2030 年,沙特阿拉伯希望追踪在国内和国际上注册供人类使用的所有药品和保健产品。到 2030 年,卫生监管机构仍将是卫生部,因为“就许多中心、服务人口规模和复杂性而言,这将是世界上最大的医疗保健转型之一。”
沙特药品食品管理局 (SFDA) 发布了药品条形码规范 6.1 版,其中提供了有关最新序列化和汇总要求及建议的信息。 SFDA 认为,从制造到患者交付的标准化识别系统对于满足日益增长的产品完整性和可追溯性需求至关重要,支持 GS1 标准的实施。
主要的反对意见指向以下方向:
![]() 提高患者安全
提高患者安全
![]() 减少用药错误
减少用药错误
![]() 启用对供应链中每个药物单元的跟踪,这将导致:
启用对供应链中每个药物单元的跟踪,这将导致:
- 检测假冒产品
- 确保可追溯性和快速的产品召回和撤回
- 确保利益相关者之间准确、实时的信息流
- 支持药物的最佳使用
序列化要求
所有药品的标记必须从线性条码升级为 GS1 数据矩阵条码,包括以下内容:
- 全球贸易项目代码
- 到期日
- 批号
- 序列号
聚合要求
制造商需要对不同的包装级别进行汇总,以便分销商到供应链更容易跟踪并向 SFDA 报告每个药物移动单元,而无需扫描单个药物盒。
- 二次包装——GTIN、有效期、批号、每个盒子上的唯一序列号
- 纸箱/箱包——用 SSCC 或 GTIN + SN 编码的线性条形码或 GS1 数据矩阵; GTIN + SN 将仅用于同质案例/卡通
- 托盘——用 SSCC 或 GTIN +SN 编码的线性条形码或 GS1 数据矩阵; GTIN +SN 将仅用于同质托盘
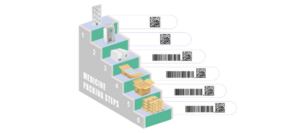
* 同质:纸箱或托盘将仅包含相同类型的药物。
** 异类:纸箱或托盘将包含不同类型的药物。
产品列表
需要使用条码进行序列化和聚合的产品有:
- 包装好的待售人用药品
- 包装好并准备出售的草药和保健品将来需要条形码。
- 包装好并准备上市销售的兽药产品将来都需要条形码。
豁免包括医药产品的免费样品、医院为特定患者和特定数量订购的非注册药物、获准供个人使用的药物以及为重新包装目的而移除的药物。
资料来源:
https://www.sfda.gov.sa/sites/default/files/2021-03/DrugBarcodingSpecificationsEN.pdf





